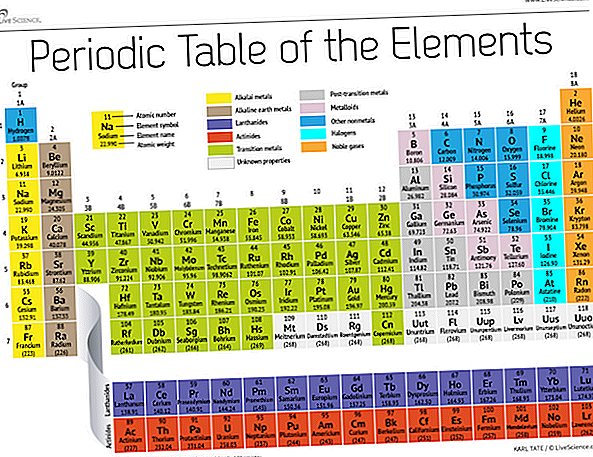
19 세기 후반, 러시아 화학자 인 드미트리 멘델레예프 (Dmitri Mendeleev)는 원자량에 따라 화학 원소를 그룹화하려는 첫 번째 시도를 발표했습니다. 당시에는 약 60 개의 요소 만 알려져 있었지만 멘델레예프는 요소가 무게로 구성 될 때 특정 유형의 요소가 규칙적인 간격 또는 주기로 발생했음을 깨달았습니다.
150 년이 지난 오늘날 화학자들은 공식적으로 118 개의 요소 (2016 년에 4 명의 새로 온 사람들이 추가 된 후)를 인정하고 멘델레예프의 주기율표를 사용하여 구성합니다. 표는 가장 간단한 원자 인 수소로 시작한 다음 나머지 원소를 원자 번호 (각 원소에 포함 된 양성자 수)로 구성합니다. 소수의 예외를 제외하면 원소의 순서는 각 원자의 질량 증가와 일치합니다.
테이블에는 7 개의 행과 18 개의 열이 있습니다. 각 행은 하나의 기간을 나타냅니다. 원소의주기 수는 얼마나 많은 에너지 레벨이 전자를 수용 하는지를 나타냅니다. 예를 들어 나트륨은 세 번째 기간에 있으며, 이는 나트륨 원자가 일반적으로 처음 세 에너지 수준에서 전자를 갖음을 의미합니다. 테이블을 아래로 이동하면 더 크고 복잡한 외부 수준을 채우기 위해 더 많은 전자가 필요하기 때문에 기간이 더 길어집니다.
테이블의 열은 요소의 그룹 또는 패밀리를 나타냅니다. 그룹의 원소는 가장 바깥 쪽 껍질에 같은 수의 전자가 있기 때문에 종종 모양과 행동이 비슷합니다. 예를 들어, 표의 가장 오른쪽에있는 그룹 18 요소는 완전히 외부 껍질을 가지고 화학 반응에 거의 참여하지 않습니다.
요소는 일반적으로 금속 또는 비금속으로 분류되지만 둘 사이의 구분선은 흐릿합니다. 금속 요소는 일반적으로 우수한 전기 및 열 전도체입니다. 금속 내 하위 그룹은 이러한 컬렉션의 유사한 특성과 화학적 특성을 기반으로합니다. Los Alamos National Laboratory에 따르면 주기율표에 대한 설명은 일반적으로 허용되는 요소 그룹을 사용합니다.
알칼리 금속 : 알칼리 금속은 표의 첫 번째 열인 그룹 1의 대부분을 구성합니다. 칼로자를 수있을 정도로 반짝이고 부드러운이 금속은 리튬 (Li)으로 시작하여 프랑슘 (Fr)으로 끝납니다. 또한 매우 반응성이 높고 물에 닿으면 불꽃이 터지거나 폭발 할 수 있으므로 화학자는 오일이나 불활성 가스에 저장합니다. 단일 전자를 갖는 수소도 그룹 1에 있지만 가스는 비금속으로 간주됩니다.
알칼리 토금속 : 알칼리 토금속은 베릴륨 (Be)에서 라듐 (Ra)까지 주기율표의 그룹 2를 구성합니다. 이 원소들은 각각 가장 바깥 쪽 에너지 레벨에 두 개의 전자를 가지고있어 알칼리 토가 자연적으로 거의 발견되지 않을 정도로 충분히 반응성이 있습니다. 그러나 그들은 알칼리 금속만큼 반응성이 없습니다. 그들의 화학 반응은 일반적으로 알칼리 금속에 비해 더 느리게 발생하고 적은 열을 생성합니다.
란탄 족 : 세 번째 그룹은 세 번째 열에 맞추기에는 너무 길어서 테이블의 맨 아래에 떠있는 섬의 맨 윗줄이되기 위해 옆으로 뒤집어졌습니다. 이것은 란타나 이드, 원소 57 내지 71-란타늄 (La) 내지 루테튬 (Lu)이다. 이 그룹의 요소는 은빛 흰색이며 공기와 접촉하면 변색됩니다.
악티늄 족 : 악티늄 족은 섬의 맨 아래 줄을 이루고 원소 89, 악티늄 (Ac), 103부터 로렌슘 (Lr)을 포함한다. 이 원소들 중에서 토륨 (Th)과 우라늄 (U)만이 지구상에서 상당한 양으로 자연적으로 발생합니다. 모두 방사성입니다. 악티늄 족과 란탄 족은 함께 내부 전이 금속이라고 불리는 그룹을 형성합니다.
전이 금속 : 표의 본체로 되돌아 가면, 그룹 3 내지 12의 나머지는 나머지 전이 금속을 나타낸다. 단단하지만 가단성, 광택 및 우수한 전도성을 가진이 요소는 금속이라는 단어를들을 때 일반적으로 생각하는 것입니다. 금,은, 철 및 백금을 포함한 금속 세계에서 가장 큰 히트 곡이 여기에 산다.
전이 금속 : 비금속 세계로의 도약에 앞서, 공유 된 특성은 세로 그룹 선을 따라 깔끔하게 나뉘 지 않습니다. 전이 금속은 알루미늄 (Al), 갈륨 (Ga), 인듐 (In), 탈륨 (T1), 주석 (Sn), 납 (Pb) 및 비스무트 (Bi)이며, 이들은 13 족 내지 17 족에 이른다. 이들 원소는 전이 금속의 고전적인 특성 중 일부를 갖지만, 다른 전이 금속보다 부드러 우면서도 열악한 경향이있다. 많은 주기율표는 대각선으로 연결되는 붕소 아래에 굵은 "계단"선이 있으며 아스타틴이 있습니다. 전환 후 금속은이 라인의 왼쪽 아래에 모입니다.
메탈 로이드 : 메탈 로이드는 붕소 (B), 실리콘 (Si), 게르마늄 (Ge), 비소 (As), 안티몬 (Sb), 텔 루륨 (Te) 및 폴로늄 (Po)이다. 그들은 금속에서 비금속으로의 점진적인 전이를 나타내는 계단을 형성합니다. 이러한 요소는 때때로 도체가 아닌 반도체 (B, Si, Ge)로 작동합니다. 메탈 로이드는 "반 금속"또는 "가난한 금속"이라고도합니다.
비금속 : 계단의 오른쪽 상단에있는 다른 모든 것-그룹 1에서 다시 시작된 수소 (H)는 비금속입니다. 여기에는 탄소 (C), 질소 (N), 인 (P), 산소 (O), 황 (S) 및 셀레늄 (Se)이 포함됩니다.
할로겐 : 불소 (F)에서 아스타틴 (At)에 이르는 그룹 17의 상위 4 개 원소는 비금속의 두 가지 하위 집합 중 하나를 나타냅니다. 할로겐은 화학적으로 매우 반응성이 있으며 알칼리 금속과 쌍을 이루어 다양한 유형의 염을 생성하는 경향이 있습니다. 예를 들어, 주방의 식탁 용 소금은 알칼리 금속 나트륨과 할로겐 염소의 결혼입니다.
고귀한 가스 : 무색, 무취 및 거의 완전히 비 반응성 인 불활성 또는 희귀 가스가 그룹 18의 표를 완성합니다. 많은 화학자들은 새로 명명 된 4 가지 원소 중 하나 인 오가네 손이 이러한 특성을 공유 할 것으로 기대합니다. 그러나이 요소의 반감기 측정 시간은 밀리 초이므로 아무도 직접 테스트 할 수 없었습니다. Oganesson은 주기율표의 7 번째주기를 완료하므로, 누군가가 원소 119를 합성 할 경우 (그리고 경쟁이 이미 진행중인 경우), 알칼리 금속 컬럼에서 8 행을 시작하기 위해 반복됩니다.
주기율에 의해 생성 된주기적인 특성으로 인해 테이블 이름을주기 때문에 일부 화학자들은 멘델레예프의 테이블을 원으로 시각화하는 것을 선호합니다.
추가 자원:












